
Volt egyszer egy sejt...
Volt egyszer egy sejt, és...-kezdődik a mese. De hogyan folytatódik, milyen sorsuk van a sejtjeinknek? Hogyan osztódnak? És legfőképp mi a történet vége?! Ezek már megint olyan kérdések, amikre a válaszok korántsem olyan egyszerűek, mint amilyennek első pillantásra tűnnek. Kezdjük az elején: szervezetünk sok milliárd sejtből épül fel. A legelső bejegyzésekben megismerkedtünk kommunikációjukkal, most pedig bemutatnék néhány sejtsorsot, azt, hogyan zajlik a sejtosztódás körvonalakban és, hogyan zajlik szabályozott körülmények között a sejthalál. Először is, az a sok milliárd sejtünk mindössze egy sejtből származik: a hímivarsejt és a a petesejt összeolvadásából képződő zigótából. Az egyedfejlődés elején a zigóta osztódásba kezd, és sok hasonló küllemű sejt keletkezik belőle. Majd ezekben a sejtekben bizonyos gének eltérő módon aktiválódnak. Ezekről a génekről majd olyan fehérjék fognak keletkezni, amik befolyásolni fogják a sejtek alakját, működését, helyzetét. Ezek a fehérjék vagy közvetlenül ugyanabban a sejtben a DNS bizonyos részeihez fognak kötődni, és befolyásolni a messenger RNS átírását, így a fehérje képződését (ezeket hívjuk transzkripciós faktoroknak). Vagy kikerülve a sejtből hatni fog a saját magára (autokrin) vagy a szomszédos sejtekre (parakrin), ilyenek például bizonyos növekedési faktorok. Nos, ezek a faktorok, peptidek, fehérjék, esetleg lipidek irányítani fogják a sejtek mozgását, és azt, hogy a megfelelő helyen megfelelő sejtek képződjenek belőle.
Nagyon fontos transzkripciós faktorokat kódoló gének a homeobox gének, amiket először az ecetmuslicában írtak le, aztán hasonló fehérjéket találtak a legtöbb állatban, az emberben is. Ezek fogják például megszabni azt, hogy a muslicának, hol legyen a szárnya, és legyen-e egyáltalán. A növekedési faktorok, pedig olyan fehérjék, amelyek a sejtből kikerülve kötődnek a receptoraikhoz, és ezzel a kötődéssel a sejtek osztódását fogják stimulálni vagy éppen gátolni. Ez nagyon finoman és pontosan szabályozott folyamat.
Ha a sejteket olyan ingerek érik, amelyek pontosan meghatározzák, hogy pl. ebből a sejtből porc vagy csontsejt legyen, akkor ezek a sejtek elköteleződnek. És soha többé nem lehet belőlük például idegsejt. Vannak olyan sejtjeink azonban, amelyek mindvégig képesek maradnak felnőtt egyedben is erre a képességre teljesen vagy legalább részben. Ezek az őssejtek. Nagyon fontos, hogy elkülönítsük az embrionális őssejteket, a felnött csontvelői őssejtektől. Ezekről napjainkban nagyon sokat lehet hallani. Olyannyira, hogy a Nature című lap online kiadása külön foglalkozik velük, mint központi téma. És persze sokan vissza is élnek vele. Azt hiszem, nem kell emlékeztetnem szinte senkit a mostani őssejtfokozós botrányra. Nagyon szép az, hogy ha az őssejteket viszünk be a beteg szövetbe, akkor ugye pótolhatjuk károsodott szöveteinket stb. Igen, ez valóban nagyon szép. Vannak már szép eredményeket elért klinikai kísérletek: pl. őssejt beültetés infarctusos szívizomba vagy nagyszerű, továbbfejleszthető laboratóriumi kísérletek erre vonatkozóan, amik egyszerűen csodálattal töltenek el. Dinamikusan fejlődő terület, lesz néhány Nobel-díj kiosztva. Lassacskán képesek leszünk -ahogy egyre jobban megismerjük a szabályozó mechanizmusokat, működési elveket, részleteket- egyszer sejtekből szervet előállítani. Persze, ez még a jövő zenéje, de biztos vagyok benne, hogy sikerülni fog. Vannak egyébként próbálkozások több-kevesebb sikerrel. De azonban meg kell jegyeznem, hogy, aki ezeket a dolgokat nyerészkedésre, átverésre használja (a vitaindító írás címe: http://szkeptikus.blog.hu/2007/07/05/rakot_okozhat_az_uj_magyar_ossejtkapszul ), ellenőrizetlenül nem túl etikus dolog, sőt...Azt hiszem sokan tudják, melyik botrányra gondolok.
Ugyanis ennek van egy másik oldala is. Mégpedig az, hogy a sejtek osztódása nagyon finoman szabályozott, érzékeny folyamat. Ha egy sejt a nyugalmi állapotából átlép a sejtciklusba, akkor két dolog történhet vele: vagy osztódik, vagy meghal. Miért is van szükség sejthalálra? A legegyszerűbb példával élve: a sejtek DNS állománya károsodhat és megjelenhetnek olyan fehérjék emiatt, amik pl. ellenőrizetlen sejtosztódást, sejtburjánzást váltanak ki. Ilyenek lehetnek növekedési faktor receptoroknak vagy éppen a receptor által elindított folyamat résztvevő fehérjéinek a mutációjából fakadó szerkezetváltozás. És emiatt például túl sokáig van érvényben a sejtosztódást serkentő szignál. Az ellenőrizetlen sejtosztódás, pedig daganat kialakulásához vezet. Azonban számos védő mechanizmus van jelen a sejtekben, hogy ez ne következzen be. Ilyen például a p53 vagy a retinoblastoma fehérjéink. Ezek nagyon fontos szerepet játszanak abban, ha ilyen káros jeleket észlel a sejt, a sejtciklus ellenőrző pontjain leállítják a sejtosztódást. Ilyenkor vagy ki tudja javítani a sejt a hibát (pl. DNS hibajavítás), vagy nem és akkor elpusztul.
A sejt életben maradását, halálát nagyon finom egyensúly szabályozza. Ezt leginkább úgy képzelhetjük el, hogy vannak olyan fehérjék, amik a sejtet életben tartják és vannak olyanok, amik a sejt halálát segítik elő. Ha több van a halál molekulákból, akkor a sejt elindul az apoptosis útján, és annak vége az, hogy a sejt DNS-e szétdarabolódik, kis csomagocskákba kerül, majd a sejt maradványait a környező falósejtek szépen bekebelezik. Így nem alakul ki a környéken gyulladás. Ha a sejt nem ilyen szabályozottan pusztul el, azt hívjuk necrosisnak. Ha ez történik a sejtalkotók kiszabadulnak, és gyulladást idéznek elő. Ha inkább több az életet jelentő molekula (pl. a limfocitáknak az antigén jelenléte ilyen), akkor a sejt túlél. Mindennap nagyon sok sejtünk hal el és osztódik, a halál és az osztódás egyensúlya tartja fent a szervezetünket, egy közel állandó sejtszámot biztosítva. Illetve a programozott sejthalál véd a daganatok kialakulásától is. Tehát a mesének a vége nagyon sokféle lehet, de a minden jó, ha a vége jó alapon történik, talán az lesz a legjobb...
Mérföldkő az őssejtkutatásban
Sikerült átprogramozni már differenciálódott sejteket -a kísérleteket a bőr kötőszöveti sejtjeivel (fibroblastok) végezték -őssejtekké, adta hírül a New Scientist.
Ezt két egymástól független kutatócsoport, egy japán és egy amerikai publikálta a Cell és a Science folyóiratokban. Már előzőleg kimutatták, hogy egerekben mindez lehetséges volt, mégis hogyan?
Ezeket a géneket mesterségesen juttatták be egy retrovirális vektor segítségével. A retrovirális vektor az egy olyan vírus, amelynek az örökítőanyaga RNS. Ebbe az örökítőanyagba építették bele a 4 gént, ami egy reverz transzkriptáz nevű enzim segítségével (ami a retrovírusok tartozéka) beépül az adott sejt eredeti DNS-be, megváltoztatva ezzel a sejt génösszetételét, és így a fehérjeszintézist. Számos vírus rendelkezik ilyen képességgel, ilyen többek között a HIV-vírus is. Azonban a retrovirális vektor mutagén hatású, így meg kell találni azt a megfelelő vektort, amivel ez csökkenthető és terápiában így felhasználható. Ez a 4 gén transzkripciós faktorokat kódol, pontosan a c-myc, Sox2, Oct-3/4 és a Klf4 nevűt. A transzkirpciós faktorok olyan fehérjék, amelyek hatással vannak más gének kifejeződésére, így a sejtek működését befolyásolják. Előzőleg kimutatták, hogy egérben differenciálódott sejteket megfertőzve embrionális őssejt tulajdonságaival rendelkező sejtek alakultak ki. Ezeket indukált pluripotens sejteknek nevezték el. Ezen a sejtek külleme, osztódása, génkifejeződése, biokémiai, molekuláris aktivitásuk az embrionális őssejtekével egyezett meg.
Az Oct3/4 és a Sox2 bizonyult a fő transzkripciós faktornak, amelyek meghatározzák az őssejtek pluripotens képességét. A pluripotencia azt jelenti, hogy többféle sejtté képesek alakulni, nincsenek elköteleződve valamely sejttípus iránt. Ezek a transzkripciós faktorok felnőtt sejtben is jelen vannak, de a célgénjeikhez nem tudnak kötődni, mert vannak olyan gátló mechanizmusok, amik ezt megakadályozzák (pl. a hisztonok módosítása acetil csoporttal vagy DNS-metiláció). A c-myc és a Klf4 gén módosította a kromatin szerkezetét, így a gátlás megszűnt. A c-myc gén képes szabályozni ezeknek a sejteknek a pluripotens képességét.
Ennek a felfedezésnek nagyon nagy jelentősége van. Ugyanis embrionális őssejteket vagyunk képesek így előállítani saját sejtekből, amiket eddig még csak embriókból sikerült izolálni. Azonban ez súlyos etikai problémákat vetett fel, sok vallásnak, egyháznak nem tetszett. Így ezeket a sejteket fel tudjuk használni, majd különféle szervek, szövetek pótlására, hiszen ezek a sejtek ismét képesek lettek más szövetekké szervekké alakulni. Előnyös az is, hogy saját sejtekről van szó.
Így olyan betegségekben, mint szívizom infarctus, Parkinson-kór, cukorbetegségben esetleg hasnyálmirigy béta sejtjeinek a pótlása, különféle érbetegségek pl. perifériás artériás betegségek ez a technika felhasználható lesz.
Az őssejtek nyomában
Manapság rengeteget hallani az őssejtekről, és tényleg már lassan a csapból is őssejtek folynak. Azonban tudjuk-e, hogy ezek a sejtek mire is szolgálnak valójában? Először is szögezzük le, hogy ebben a bejegyzésben kizárólag csontvelői és perifériás vérben lévő őssejtekről lesz szó, amelyek nagymértékben különböznek az embrionális őssejtektől.
A csontvelőnek két megnyilvánulási formája létezik. Az egyik a sárga csontvelő, amely zsírsejteket tartalmaz, és ennek nem létezik vérképző funkciója. Azonban bizonyos hatásokra átalakulhat vörös csontvelővé, ami a vérképzés színhelye. Felnőtt korban a vörös csontvelő a lapos csontokban fordul elő. Ilyen a például a csípőlapát. Gyermekkorban, a csöves csontokban is vörös csontvelő van és ez sárga csontvelővé alakul a későbbiekben.
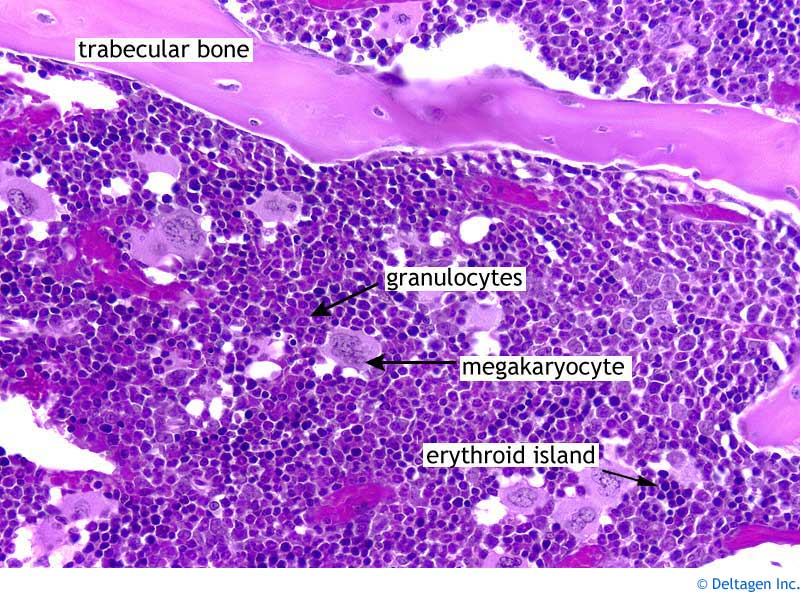
Miből is áll a vörös csontvelő?
A vörös csontvelő áll strómasejteknek nevezett sejtekből, amelyeknek fontos szerepük van a különböző vérsejtek érésében. Itt találhatóak a különböző vérsejt előalakok, amelyek a csontvelői őssejtekből jönnek létre. Ezek az őssejtek úgy osztódnak, hogy egy vérsejt előalak képződik belőlük és egy másik őssejt. Ezt nevezzük asszimmetrikus osztódásnak. Az őssejtek szerepéről még szólni fogok, és szeretnék eloszlatni néhány tévhitet is velük kapcsolatban. A régebben csak térkitöltőnek hitt zsírsejtek is találhatóak itt. Azonban ma már tudjuk, hogy a zsírsejtek számos olyan anyagot termelnek, amelyek hatással lehetnek akár ezeknek a sejteknek a differenciálódására és különböző immunológiai folyamatokra is.
Milyen sejtek is alakulnak ki itt?
A vér alakos elemei mind itt alakulnak ki egy többlépcsős folyamaton keresztül, amelyet most nem tárgyalnék, majd erre kitérhetünk a későbbiekben.
Mire használhatóak a csontvelői őssejtek az orvoslásban?
A csontvelői őssejteket felhasználhatjuk a különböző leukémiák és rákok kezelésében. Ekkor kiírták a károsodott csontvelőt kemoterápiával, és helyette a donor csontvelői őssejtjeit helyezik be. Ha a csontvelő megtapad, akkor a betegnek egy új immunrendszere tud kifejlődni. A donor lehet akár a beteg is, ezt nevezik autológ transzplantációnak. Ezt tudják különböző lymphomák és myeloma multiplex kezelésére alkalmazni. Ezek az őssejtek származhatnak a csontvelőből vagy a perifériás vérből. A másik, a köldökzsinórvérből származó őssejtek, melyeket ha születéskor levesznek, azok tárolhatóak és betegség esetén visszaadhatóak a betegbe. Ennek azaz előnye, hogy nem kell hátrányos immunreakcióra számítani, hiszen a beteg a saját sejtjeit kapja. Azonban hátránya lehet, hogy maga az őssejt is lehet már rákosan elfajult. Ebben az esetben nem lehet ezt alkalmazni. Az allogén transzplantáció pedig azt jelenti, hogy a beteg nem a saját őssejteit kapja, hanem egy olyan emberét, akinek az MHC-alléljai megegyeznek. Ennek egy speciális változata az, amikor a donor a beteg egypetéjű ikertestvére, ezt nevezik szingén transzplantációnak. Ennek az előnye az, hogy az új immunrendszer mentes a rákos sejtektől, hátránya azonban éppen abban rejlik, hogy az MHC-allélok nem minden esetben teljesen azonosak, természetesen ikertestvérek esetén ez nem áll fent, ők teljesen azonosak.
Ma már számos kísérlet folyik arra vonatkozóan, hogy a csontvelői őssejtek, nemcsak a vér sejtjeivé képesek differenciálódni, hanem például szívizommá, izommá, csonttá. Ez egyes szívinfarktusos esetekben hatásos lehet. Debrecenben történt is ilyen kezelés már, mikor a beteg csontvelői őssejtjeit adták be a károsodott szívizomba és kecsegtető eredmények vannak, lassú javulás észlelhető az elhalt területen. A másik ilyen sikertörténet lehet a különböző érszűkületes betegek ereinek a pótlása csontvelői őssejtekkel és szintén kedvező eredmények vannak ezzel kapcsolatban.
Fontos megjegyezni, hogy mostanában volt egy-két botrány mindenféle állítólagos őssejt stimuláló szerekkel kapcsolatban. Ezzel kapcsolatban csak annyit tennék hozzá, hogy bármely beavatkozás a sejtosztódásba magában hordja a rákos megbetegedések kialakulásának a kockázatát. És mindezt ellenőrizetlen termékekkel, marketingfogásokra hallgatva nemcsak, hogy felelőtlenség mással vagy éppen sajátmagunkkal szemben, hanem veszélyes is lehet.





Nincsenek megjegyzések:
Megjegyzés küldése